El trasplante renal es mejor tratamiento renal sustitutivo; ofrece mejor calidad de vida al restaurar todas las funciones afectadas y elimina la necesidad de diálisis. Un riñón trasplantado puede funcionar bien durante muchos años, dependiendo del estado de salud general del receptor y de las características del riñón trasplantado.
No obstante, antes optar a un trasplante renal se deben realizar exploraciones complementarias ya que precisa de fármacos inmunosupresores, es decir, que deprimen las defensas naturales del organismo y predisponen a otras enfermedades de carácter infeccioso. Además, esos estudios contribuirán al éxito de la cirugía, que no deja de ser una intervención quirúrgica con riesgos. De esto se deduce que no todos los pacientes son aptos para dicha intervención, debiendo ser valorado cada caso por un nefrólogo y el equipo de trasplante.
El trasplante de riñón: una alternativa de tratamiento para la Enfermedad Renal Crónica
En el presente artículo la Doctora Karina Furaz, nefrólogo del Centro de Diálisis FRIAT Los Llanos de Móstoles, hace una exhaustiva revisión del trasplante de riñón como alternativa de tratamiento para los pacientes con IRC terminal. A lo largo del texto la doctora Furaz detalla el protocolo que se sigue en España para ser candidato a trasplante, analiza sus ventajas e inconvenientes y detalla sus contraindicaciones, factores de riesgo y posibles complicaciones.
El primer trasplante de órganos exitoso fue el de riñón, realizado entre gemelos idénticos en la ciudad de Boston (EE. UU.) el 23 de diciembre de 1954. En los años en que se desarrolló la técnica del trasplante renal, entre 1965 y 1980, la supervivencia de los pacientes mejoró progresivamente hasta alcanzar el 90%, y la del injerto aumentó hasta ser mayor del 80% tras la introducción de la ciclosporina. Actualmente en receptores de primer trasplante (no sensibilizados) ya sea de donante fallecido o vivo tienen expectativas de supervivencia al año del paciente del 95% y del injerto del 90%.
Varios grupos han comunicado excelentes resultados aun en trasplantes con incompatibilidad de grupo ABO, pero incluso en pacientes hiperinmunizados debido a trasplantes previos, el desarrollo de mejores protocolos de desensibilización y los programas de intercambio pareado de riñones ofrecen hoy verdaderas oportunidades de lograr un trasplante exitoso.
Numerosos estudios han demostrado que: el trasplante renal es una terapia que mejora la supervivencia a largo plazo cuando se compara con la diálisis de mantenimiento.
El trasplante en situación de prediálisis es una opción atractiva, ya que mejora la supervivencia del injerto y reduce los costos. Se asocia a una reducción del 25% en el fallo del injerto y del 16% en la mortalidad, en comparación con los receptores que se trasplantan después de ingresar en diálisis; aunque no es posible realizarlo en todos los casos ya que va a depender del grupo sanguíneo del paciente y de la oferta de donantes.
El trasplante renal apropiadamente indicado es, por lo tanto, el tratamiento de elección para los pacientes con IRC terminal debido a que ofrece una mejor evolución de la enfermedad y a sus menores costos.
Sin que existan reglas exactas, una vez presentada la naturaleza crónica del proceso de enfermedad renal y establecida la disminución de la función renal (generalmente cuando el filtrado glomerular alcanza valores de alrededor de 30 ml/min) , se hace necesario presentar las diferentes opciones de tratamiento renal sustitutivo (TRS) a las que habrá que recurrir cuando los valores de función renal propia estén próximos a ser verdaderamente insuficientes. En ese momento el paciente deberá ser evaluado por nefrólogos en consultas específicas de prediálisis o de nefrología clínica, donde se presentarán las diferentes opciones de TRS. Entre ellas, las dos técnicas de depuración (diálisis peritoneal y hemodiálisis) y los dos tipos de trasplante de riñón (donante vivo y donante fallecido).
Existen a su vez diferentes sitios donde los enfermos pueden acceder a informarse: En España, este vehículo de información actualmente disponible en la Organización Nacional de Trasplantes (ONT) y en páginas oficiales de Fundaciones y Servicios de Salud de Comunidades Autónomas (CCAA).
Proceso de evaluación inicial:
Se valorará la competencia y grado de autonomía del paciente y se le entregará un consentimiento informado.
Se le informará sobre las posibilidades de trasplantarse un riñón de un donante vivo o cadáver, sobre los riesgos de cirugía y rechazo, complicaciones de la inmunosupresión y sobre los resultados globales del programa de trasplante de referencia.
Protocolo de evaluación y requisitos para inclusión en lista de espera de trasplante:
Depende de cada centro trasplantador (cada uno de ellos tiene sus propios protocolos) pero en líneas generales se hace el siguiente procedimiento:
- Revisión de historia clínica y psicosocial
- Exploración física rigurosa
- Pruebas analíticas, radiodiagnósticas y funcionales
- Valoración por otros especialistas, según la historia clínica del paciente (digestivo, urología, psiquiatría, etc)
La historia clínica recoge: antecedentes personales y familiares sobre la enfermedad renal de base y su afectación extrarrenal, datos de enfermedad cardiovascular, infecciones y neoplasias. También se valoran características psíquicas del paciente, en particular grado de autonomía y cumplimiento de los tratamientos prescriptos, y documenta posibles conductas de riesgo y de adicción a alcohol y/o drogas.
La enfermedad renal de base debe ser conocida y precisado su carácter familiar o no, para valorar la pertinencia de trasplante de donante vivo o cadáver y posibilidad de recidiva en el injerto.
La agudización o reactivación de infecciones como consecuencia de la inmunosupresión es una de las principales causas de morbilidad y mortalidad en le trasplante. Por eso se realizan pruebas para detección de infecciones, se analizan exposición a tuberculosis, viajes a zonas con infecciones endémicas, antecedentes de enfermedades infecciosas. Es importante conocer la historia de vacunas, y actualizar las mismas si procede. Los pacientes en diálisis y lista de espera deben estar vacunados de gripe, neumococo y hepatitis B.
Absolutas
- Neoplasia maligna reciente con actividad metastásica
- Infección activa
- Enfermedad extrarrenal irreversible sin rehabilitación o con expectativas de vida inferior a un año
- Enfermedad psiquiatrita con perdida de autonomía o competencia
- Incumplimiento terapéutico reiterado
- Adicción a drogas y/o alcohol sin posibilidades de rehabilitación
- Prueba cruzada positiva IgG frente a células T del donante
Hoy día no obstante es difícil hablar de contraindicaciones absolutas, y cada paciente debe ser valorado de forma individual y según su situación particular.
Relativas
- Edad avanzada > de 75 años
- Enfermedad cardiovascular
- Hepatopatía crónica avanzada
- Anomalías de vías urinarias
- Tumores malignos previos
- Enfermedad de base
Edad
No existe límite formal de edad para excluir a un paciente como candidato para trasplante.
La edad es uno de los criterios que más se ha flexibilizado de acuerdo con el envejecimiento de la población general y la de diálisis. No existen muchos estudios que proporcionen pruebas sobre los resultados en pacientes muy ancianos, por encima de 70 años, pero los obtenidos en receptores de más de 60 años, son mejores que los que lograrían permaneciendo en diálisis consiguiendo, en general, un grado aceptable de función renal a largo plazo.
Los pacientes ancianos tienen mayor morbilidad con tasas de hospitalizaciones más altas a los receptores más jóvenes y también mayor riesgo de enfermedad cardiovascular, neoplasias e infecciones, por lo que la evaluación debe ser muy rigurosa. Sin embargo también experimentan menos rechazo y precisan inmunosupresión menos agresiva.
Algunos grupos consideran a los pacientes muy ancianos como: candidatos preferentes a recibir riñones de donante cadáver con “criterios ampliados” (edad avanzada, obtenidos en asistolia, etc.) o ser receptores de doble trasplante con este tipo de donantes.
El trasplante de donante vivo en mayores de 65 años plantea problemas especiales que deben ser resueltos con estricto respeto a factores éticos subyacentes.
Retrasplantes e hipersensibilización HLA
Los restrasplantes (2º,3º,4º,5º trasplante), son cada vez más frecuentes, y se asocian a mayores tasas de pérdida del injerto sobre todo cuando existe historia de rechazos previos. Haber recibido inmunosupresión aumenta la incidencia de complicaciones infecciosas o neoplásicas, por lo que se reforzará las medidas destinadas a buscar cualquier eventualidad de este tipo antes de la reinclusión.
Los pacientes hipersensibilizados por transfusiones, embarazos, o trasplantes previos, se deben trasplantar con la mayor compatibilidad HLA posible dada sus características. En España y Portugal existe una lista única estatal de receptores hipersensiblizados a los que se le da preferencia para trasplante con donante cadáver, pero a pesar de tener preferencia el tiempo en lista de espera se suele alargar.
Obesidad
Pacientes con índice de masa corporal superior a 30 kg/m2 tienen mayor incidencia de complicaciones quirúrgicas, de retraso de cicatrización, lo que motiva estancias hospitalarias más prolongadas.
Hay resultados controvertidos respecto a la asociación de obesidad con disminución de la supervivencia de los injertos. Sin embargo la obesidad es un factor de riesgo para el desarrollo de diabetes, enfermedad cardiovascular e hiperfiltración post trasplante.
Por lo que se recomienda una pérdida de peso significativa antes de inclusión en lista de espera.
Enfermedad cardiovascular
La cardiopatía isquémica es la principal causa de muerte en los pacientes trasplantados y de pérdida del injerto con función adecuada.
El riesgo de padecer enfermedad cardiovascular es mayor en: pacientes con enfermedad cardiovascular previa, diabéticos, fumadores, obesos (IMC superior a 30), portadores de factores de riesgo cardiovascular clásicos, edades mas avanzadas, evolución de insuficiencia renal muy prolongada, y en los que tienen hipertensión arterial mal controlada e hipertrofia ventricular izquierda.
La evaluación de la cardiopatía isquémica es muy importante sobre todo en diabéticos, en los cuales la enfermedad coronaria con frecuencia es asintomática. Lo pacientes asintomáticos y de bajo riesgo se le deben tratar los factores modificables antes de incluirles en listas, Los de alto riesgo (infarto previo, edad avanzada diabetes,) aunque estén asintomáticos, se les realizará pruebas de tolerancia de stress(ergometría, ecografía con dobutamina, gamagrafia con talio dipiridamol, RNM o TAC. Lo paciente con pruebas no invasivas positivas y los sintomáticos se estudiarán con coronariografía.
Pacientes con enfermedad coronaria grave y difusa no susceptible de revascularización o con insuficiencia cardíaca grave, no son buenos candidatos para trasplante renal, y según el caso se puede valorar el doble trasplante corazón riñón.
Si existe historia previa o presencia de factores de riesgo de enfermedad cerebrovascular se realiza dopler de carótidas y cirugía si precisa. También se usa el dopler para evaluar circulación periférica en pacientes diabéticos o con claudicación intermitente.
Infecciones
Se tratan las infecciones activas antes de meter en lista a un paciente.
Los pacientes con HIV: pueden ser incluidos siempre que tengan carga viral indetectable, recuento de células T normales y buena tolerancia al tratamiento antiviral.
La infección por Citomegalovirus es una de las principales causas de morbilidad en el trasplante por lo que es imprescindible detectar la presencia de anticuerpos CMV en todos los pacientes en lista de espera y realizar posteriormente una profilaxis adecuada.
Varicela Zoster: se les debe hacer serología antes de la inclusión en lista, y los pacientes que no tengan anticuerpos IgG específicos antes del trasplante serán vacunados y se administrara inmunoglobulinas específicas a los expuestos al virus después del trasplante, para evitar desarrollo de enfermedad fulminante.
Virus C: no es contraindicación para el trasplante. Se les determina RNA VHC y se les efectúa biopsia hepática. Los pacientes con fibrosis en puente o cirrosis se excluyen como candidatos o se les propone valorar para trasplante hepato-renal.
Virus B: Los resultados en pacientes con antígeno de superficie positivo son inferiores a los obtenidos en otros pacientes. Los pacientes con datos de replicación viral, coinfección por virus C o D y los que tienen elevación persistente de transaminasas tienen peor pronóstico.
La mayoría de los grupos propone la realización de biopsia hepática. Los pacientes sin datos de replicación viral y sin datos de hepatitis crónica activa son candidatos.
La inmunosupresión favorece la reactivación de la tuberculosis y su diseminación. Todos los pacientes se les deben descartar enfermedad y ser portadores de una RX de tórax. Los pacientes con infección activa deben recibir tratamiento completo, y los que han tenido una infección previa quimioprofilaxis.
Diabetes
El trasplante renal en pacientes diabéticos se puede realizar siempre que no exista una grave enfermedad vascular que contraindique esta terapéutica. La morbimortalidad de estos pacientes es mayor que la de la población no diabética. En los pacientes con diabetes tipo I, se puede indicar el doble trasplante de páncreas-riñón y en los diabéticos tipo II, el trasplante de riñón. En ambos grupos de pacientes el estudio pretrasplante debe ser muy riguroso, haciendo especial énfasis en el estado cardiovascular.
Tumores malignos
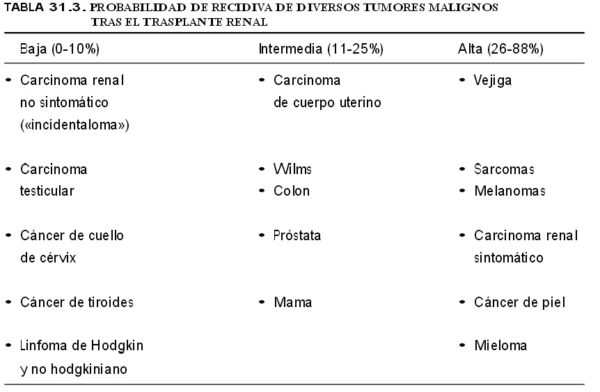
Los receptores que padezcan o que hayan presentado un tumor maligno recientemente deben ser excluidos de la lista de espera para trasplante renal. Si el tratamiento del tumor ha sido efectivo y han transcurrido entre 2 y 5 de seguridad sin recidiva (dependiendo del tipo y extensión del tumor), se puede replantear la posibilidad del trasplante renal, siempre que el paciente conozca y acepte que la probabilidad de reactivación tumoral existe y que la inmunosupresión la puede favorecer.
En la tabla quedan reflejadas las probabilidades de recidiva de diversos tumores malignos tras el trasplante renal.
Anomalías del tracto urinario
Los pacientes con problemas urológicos precisan evaluación específica por urología. La mayoría de las veces la cirugía del trasplante no precisa de nefrectomía previa de los riñones del paciente. Las indicaciones de nefrectomía previas al trasplante se reflejan en la siguiente tabla:

Enfermedad pulmonar
Se debe evaluar la existencia de cualquier enfermedad pulmonar que complique la anestesia y la cirugía en el trasplante por infección y dependencia ventilatoria o que pueda comprometer su evolución, ya que la inmunosupresión incrementa la frecuencia y gravedad de las infecciones.
No hay protocolos estandarizados de estudio y manejo de pacientes con enfermedad pulmonar, aunque es imprescindible realizar una espirometría.
Enfermedad gastrointestinal
Los pacientes con antecedentes de diverticulitis son evaluados cuidadosamente y en ocasiones necesitan colectomía parcial previo al trasplante.
La colelitiasis es frecuente en los pacientes en lista de espera principalmente los diabéticos .La colecistectomía está indicada si hubo episodios previos de colecistitis para evitar su recurrencia.
En los pacientes con historia de pancreatitis se controlan los factores de riesgo modificables como: la hipercalcemia, consumo de alcohol, colelitiasis y dislipemia.
Los pacientes con úlcera péptica activa no pueden trasplantarse hasta ser tratados adecuadamente, debido al alto riesgo de perforación por el uso de altas dosis de esteroides. Los pacientes sintomáticos se les estudia para descartar infección por Helicobacter pylori y se les realiza endoscopia.
Trastornos de coagulación
Los pacientes con historia de trombosis (incluida las trombosis recurrentes de fístulas) se estudian para descartar estados de hipercoagulabilidad, que pueden provocar pérdida del injerto.
Cuando existan anomalías tratables se decide con hematología la mejor opción terapéutica.
Enfermedad de base
En todos los enfermos candidatos a trasplante renal hay que plantearse la posibilidad de recidiva de la enfermedad original que causó la insuficiencia renal terminal. Afortunadamente, menos del 5% de los injertos fracasan por recidiva de la enfermedad primaria. En la tabla queda reflejada la posibilidad de recidiva de nefropatías primarias y secundarias tras el trasplante renal. En la práctica, el problema se plantea con la oxalosis, ya que la recurrencia es del 100%; el tratamiento adecuado es el doble trasplante hepático y renal. También con la glomerulosclerosis focal de rápida evolución, fundamentalmente cuando ya ha presentado una recidiva precoz y grave en el primer trasplante. En estos casos el segundo trasplante debe valorarse cuidadosamente dado que la probabilidad de recurrencia es del 80%.
Complicaciones quirúrgicas
Estas suelen ocurrir en los primeros días post trasplante, y pueden ser:
Del parenquima
- Rotura renal
- Traumatismo renal
Urológicas
- Fístulas
- Estenosis de uréter
- Reflujo vesicoureteral
- Litiasis
- Hematuria
- Infección urinarias
Vasculares
- Estenosis de la arteria renal
- Trombosis arterial
- Trombosis venosa
- Fistula artriovenosa
- Aneurisma de la arteria renal
- Hemorragia
Linfocele
De la herida quirúrgica
- Seroma
- Infección
- Hematoma
- Evisceración
- Eventración
Complicaciones médicas
Agudas
Necrosis tubular aguda (NTA): La NTA es la principal causa de disfunción aguda del injerto renal en el post- operatorio inmediato, afectando entre un 15 y un 40% de los trasplantes de donante cadáver y a menos de un 5% de los de donante vivo.
Rechazo agudo: Los nuevos inmunosupresores principalmente micofenolato mofetil y tacrolimus han reducido considerablemente su incidencia (inferior al 20%) y gravedad. Aparece habitualmente a partir de la primera semana, en general, durante los 3 primeros meses. No obstante, puede aparecer en cualquier momento evolutivo, inclusive en fases tardías (muchas veces a consecuencia de un mal seguimiento del tratamiento por parte del paciente).
Rechazo hiperagudo (RHA): Se diagnostica en el mismo acto operatorio en el que el riñón no adquiere la consistencia normal, aparece edematoso y de coloración azulada, como consecuencia de coagulación intravascular en el injerto. Es, hoy en día, excepcional desde que se generalizara la prueba cruzada pretrasplante; sin embargo, cuando se produce es habitualmente intratable e irreversible.
Rechazo acelerado
Toxicidad renal por tacrolimus o ciclosporina
Infecciones: constituyen las complicaciones agudas con mayor impacto en términos de morbilidad y mortalidad en el paciente trasplantado. Se relacionan con: edad del paciente, situación nutricional y urémica (p. ej., adecuación de la diálisis pretrasplante) y presencia de diabetes mellitus; patologías infecciosas sobreañadidas (p. ej., infección por el virus de la hepatitis B o C); protocolo de inmunosupresión administrado ; presencia de complicaciones quirúrgicas ; necesidad de sondajes o cateterismos; grado de función renal; presencia de leucopenia y exposición epidemiológica a diversos agentes (p. ejemplo, serología CMV de donante y receptor; agentes nosocomiales, etc.).
Complicaciones cardiovasculares: las enfermedades cardiovasculares constituyen la principal causa de mortalidad a largo plazo en el paciente trasplantado renal, destacando la elevada prevalencia de hipertensión arterial y de hiperlipidemia en los pacientes nefrópatas y trasplantados renales. No menos del 75% de los pacientes trasplantados muestran hipertensión arterial. Los esteroides y anticalcineurínicos, ciclosporina y tacrolimus, que están presentes en la mayoría de protocolos de inmunosupresión contribuyen asimismo al desarrollo de HTA.
Complicaciones digestivas y hepáticas. Con la administración de dosis bajas de esteroides con los actuales protocolos de inmunosupresión y la generalización del empleo de antihistamínicos H2, especialmente en pacientes con sintomatología o historia previa de ulcus, en las primeras semanas postrasplante, las complicaciones pépticas son actualmente poco frecuentes.
La pancreatitis aguda es una complicación grave, cuya incidencia en la población trasplantada oscila entre el 0,5 y el 4%, habiéndose relacionado con la toma de esteroides y ciclosporina, con la infección por CMV, enfermedad hepatobiliar y con la ingesta de alcohol.
Entre las complicaciones del colon destaca la aparición de colitis en el seno de enfermedad invasiva por CMV, así como el riesgo de perforación en pacientes afectados de diverticulitis aguda.
Las complicaciones hepáticas derivadas de la infección por el virus de la hepatitis B o C aparecen en evoluciones a medio y largo plazos. Cabe, no obstante, la posibilidad de que en el seno de tratamientos inmunosupresores enérgicos puedan acelerar el curso de la hepatopatía o incluso desarrollar una hepatitis fulminante. Asimismo, en este grupo de pacientes se ha señalado un riesgo de morbilidad y mortalidad aumentada debida a complicaciones infecciosas, lo que se ha relacionado con la capacidad inmunomoduladora de los citados virus.
Resulta más frecuente, en la fase aguda del postrasplante, la aparición de elevaciones enzimáticas autolimitadas (hepatitis) por toxicidad de fármacos, fundamentalmente ciclosporina, o en el seno de la infección por CMV.
Neoplasias en fase precoz: pueden estar en relación con neoplasias latentes en el receptor que se ponen de manifiesto tras el trasplante o con la transmisión del donante con el injerto. También pueden desarrollarse procesos linfoproliferativos o sarcomas de Kaposi en el primer semestre postrasplante, por lo que deberán tenerse presente estas posibilidades.
Hiperparatiroidismo secundario: se sigue frecuentemente de hipercalcemia e hipofosfatemia, en la mayoría de los casos autolimitadas.
Alteraciones hematológicas. Suelen verse con frecuencia en las etapas precoces postrasplante, anemia y/o leucopenia, fundamentalmente. Las alteraciones hematológicas pueden ser también consecuencia de infecciones ,tales como el CMV o linfoma.
Recidiva de nefropatías originarias: Ya explicado anteriormente.
Complicaciones crónicas:
HTA grave: la hipertensión arterial (HTA) postrasplante se presenta entre un 60-80% de los casos, según las series. Tras el trasplante renal, la HTA incrementa la morbimortalidad cardiovascular del receptor y empeora la supervivencia del injerto a largo plazo.
Osteopatía post trasplante: en gran parte ocasionada por el uso crónico de esteroides.
Hipercalcemia
Hipofosfatemia
Pérdida de masa ósea
Ocurre de forma más acusada durante los 6 a 18 primeros meses postrasplante. Los estudios en pacientes trasplantados más a largo plazo ofrecen, sin embargo, resultados más contradictorios. El factor fundamental en el desarrollo de osteopenia es el uso de glucocorticoide.
Osteonecrosis
Sindromes linfoproliferativos. Los síndromes linfoproliferativos (SLP) son los cánceres de novo más frecuentes en los receptores de trasplante renal, después de los tumores de piel y labios (no melanomas). Tienen su mayor incidencia en el primer año del período postrasplante.
El número de trasplantes realizados han aumentado a lo largo de los años hasta 2.551, fundamentalmente debido al aumento del trasplante de donante vivo (14,15%) y del donante fallecido en parada cardíaca (asistolia)(7,88%).
Los países que han realizado mayor número de trasplantes son EEUU, China, Brasil e India, mientras que el mayor acceso de la población a este tratamiento se registra en Austria, EEUU, Croacia, Noruega, Portugal y España.
El 50,78 % de los pacientes con ERC están trasplantados.
Trasplante de riñón donante vivo. Información para donante y receptor
Lo primero que tienen que saber, tanto el donante como el receptor y sus familiares, es que el trasplante de donante vivo sólo estará justificado y será aceptado tras llevar a cabo un riguroso estudio de riesgo/beneficio para donante y receptor, así como una exhaustiva evaluación de acuerdo con los mejores estándares éticos.
Así mismo la información es fundamental en este proceso. Todos los agentes implicados reciben previamente, y con todo detalle, información de interés a cerca del tipo de estudios que van a acreditar la viabilidad del TRDV y la seguridad de la donación.
La experiencia mundial acumulada tras más de 50 años de TRDV permite ofrecer una elevada seguridad para la donación de uno de los riñones.
Así mismo existe unanimidad de la mejor supervivencia de injertos y pacientes en trasplante renal cuando el riñón procede de un donante vivo respecto a donante fallecido. Las razones son múltiples, entre ellas, el hecho de ser una intervención quirúrgica programada en la que tanto el donante como el receptor llegan en una situación óptima para la cirugía, la óptima calidad de los riñones trasplantados y la menor edad de los receptores.
En general el riesgo que asume un donante de riñón es inferior al que asumen otras personas que se someten a anestesia general y cirugía mayor, ya que todos los donantes tienen acreditada una buena salud. No obstante a todos ellos se les informa de los riesgos inherentes a la anestesia, la cirugía y posibles complicaciones intraoperatorias y postoperatorias, propios de cualquier intervención quirúrgica.
Así mismo se debe hacer especial hincapié en comentar con detalle las circunstancias que se pueden presentar al vivir con un único riñón, incluidos riesgos excepcionales, como pudieran ser traumatismos severos o problemas médicos infecciosos o litiásicos que pudieran comprometer la función del único riñón existente.
A largo plazo, se puede confirmar que la tendencia a pérdida progresiva del filtrado glomerular no es significativa en ningún grupo de edad; la hipertensión no aumenta en incidencia con el paso de los años e incluso las expectativas vitales serían superiores respecto a quienes mantienen los dos riñones ya que se trata de una población sana.
Respecto al embarazo en mujeres donantes, no existen riesgos adicionales descritos en las gestaciones en pacientes monorrenas por haber sido donantes de riñón, si bien se prestará especial atención a controles de la presión arterial, ganancia de peso y proteinuria, en general no diferentes de los que se pueden recomendar a otro tipo de gestantes.
La nefrectomía actual (extracción del riñón) se hace mediante laparoscopia, siendo las estancias hospitalarias son cada vez más reducidas. Los donantes deberán hacer una vida sedentaria las dos primeras semanas y pasado ese período, y según el tipo de trabajo, se valorará la reincorporación a la normalidad personal y laboral.
Las actividades deportivas pueden ser realizadas por los donantes sin ningún cuidado o limitación especial a las 6-8 semanas de la cirugía. En cualquier caso, del análisis de las grandes series de donantes se puede inferir que de mantenerse estrictos criterios de selección, la seguridad a largo plazo para el donante puede considerarse garantizada.
Los estudios de calidad de vida de los donantes de riñón aprecian mejoras en la esfera afectiva y mejoras en la percepción de calidad de vida ya que las motivaciones hacia la donación se ven continuamente reforzadas en todos los casos en los que el trasplante continúa cumpliendo su función. En el caso de cónyuges, además de una excelente supervivencia del injerto, las ventajas adicionales para el que dona se centran en la posibilidad de una vida en pareja más normal, sin las limitaciones de viajes que impone la diálisis o la comorbilidad asociada a problemas con acceso vascular u otras relacionadas con la insuficiencia renal.
Finalmente exponemos una tabla que resume los riesgos principales para el receptor del donante vivo.

El estudio integral de una donación de riñón de vivo persigue comprobar los siguientes requisitos:
- Que la donación es libre, consciente y desinteresada. Implica entre otros requisitos, que el donante: a) no padece trastornos cognitivos o emocionales; b) goza de una capacidad intelectual y un nivel de comunicación que le permitan entender la información sobre riesgos y beneficios; c) no está sometido a presiones externas, y d) no busca recompensas materiales de cualquier tipo.
- Que el donante tiene riñones normales y el riesgo de desarrollar nefropatía a largo plazo es reducido: a) actualmente presenta función renal normal y está libre de cualquier alteración renal analítica o estructural significativa; b) ausencia de nefropatías heredofamiliares que puedan desarrollarse posteriormente, y c) no existen procesos o alteraciones que incrementen el riesgo de nefropatía, por ejemplo, enfermedades sistémicas, hipertensión arterial (HTA) severa o diabetes.
- Que el donante no presenta otras enfermedades o alteraciones que puedan: a) incrementar el riesgo quirúrgico o anestésico) verse perjudicadas por una menor reserva renal, o c) transmitirse al receptor, como cáncer o infecciones.
- Que el receptor es aceptable para trasplante: no presenta contraindicaciones, y su pronóstico vital y de rehabilitación es razonablemente bueno y mejorará de forma relevante con el TRDV.
- Que el trasplante es posible técnicamente con un riesgo aceptable: a) vasos y vías urinarias son apropiados (donante y receptor), y b) no hay incompatibilidad inmunológica
Edad: La edad mínima para la donación en nuestro país es 18 años, por motivos legales. No hay una edad límite máxima bien establecida (aunque en España rara vez se contempla la donación por encima de los 70 años).
Hábitos: El tabaquismo y el consumo abusivo de alcohol (>60g/día) pueden justificar exploraciones adicionales e incrementan el riesgo de complicaciones posquirúrgicas en general. Se recomienda fuertemente el cese completo de estos hábitos al menos 4 semanas antes de la intervención. Debería insistirse en el abandono definitivo, puesto que el tabaquismo incrementa el riesgo de mortalidad a largo plazo del donante. La adicción a drogas de abuso es una contraindicación para la donación.
Hipertensión: La tensión arterial en visitas separadas debería ser <140/90mmHg; la media de cifras en MAPA debe ser <135/85 mmHg durante el día y <120/75 mmHg durante el sueño. Es admisible la donación de un hipertenso leve o moderado sin otros factores de riesgo cardiovascular y buena función renal, siempre que se cumplan ciertas condiciones: a) edad superior a 50 años; b) no afroamericano; c) ausencia de datos de repercusión visceral de la hipertensión (ECG-ecocardiografía, fondo de ojo, microalbuminuria <30 mg/día); d) la tensión puede ser controlada mediante cambios en el estilo de vida y el uso de no más de un hipotensor, y e) existe una garantía razonable de que el donante seguirá control y tratamiento de manera indefinida. Como ocurre en la población general, la hipertensión se asocia a mayor mortalidad del donante a medio plazo. Por otra parte, y aunque hay datos conflictivos, un metanálisis reciente parece confirmar que la donación se asocia a un incremento de la tensión arterial de 5 mmHg. Además, con una selección y manejo adecuados de su hipertensión, los donantes hipertensos no parecen tener peor función renal tras la donación, al menos a corto plazo. Todo esto justificaría el empleo de donantes hipertensos leves con expectativa de vida limitada por su edad actual, si es de esperar un control adecuado.
Obesidad: La obesidad severa (IMC >35) es una contraindicación para la donación, al estar asociada a un mayor riesgo quirúrgico y de desarrollo de ERC a largo plazo. La obesidad entre 30 y 35 de IMC (o diámetro de cintura >82 cm en mujeres o >102 cm en hombres) puede constituir también una contraindicación si se asocia a otros factores de riesgo como hipertensión, glucemia basal alterada o antecedentes familiares, microalbuminuria. En todo caso debe advertirse de su posible mayor riesgo a largo plazo y orientarse al donante para que consiga la máxima reducción de peso antes de la intervención y la mantenga después indefinidamente mediante cambios en sus hábitos de alimentación.
Función renal: En pacientes por debajo de 40 años es deseable un aclaramiento >90 ml/min/1,73 m2, especialmente en sujetos obesos, mientras que muchos centros admiten aclaramientos menores (alrededor de 70 ml/min e incluso menos) en donantes de mayor edad (>60 años).
Proteinuria: Una proteinuria >300 mg/día descarta la donación. El valor de la microalbuminuria no está bien establecido respecto a la donación: una microalbuminuria >30 mg/día es una contraindicación relativa. Ante valores límite de proteinuria (150-300 mg/día) o en presencia de microalbuminuria (30-300 mg/día) se tiende a desaconsejar la donación, pero puede valorarse el caso de manera individualizada, teniendo en cuenta otros factores como edad, obesidad, hipertensión o alteración del metabolismo glucídico.
Valoración cardiovascular: Persigue descartar cardiopatías significativas que constituyen contraindicación por aumento de riesgo del donante: cardiopatía isquémica, insuficiencia cardíaca, valvulopatía, hipertrofia ventricular izquierda significativa o arritmia significativas. Adecuadamente seleccionados los donantes no parecen ver aumentado su riesgo cardiovascular postrasplante.
Diabetes y síndrome metabólico: Estudio mínimo: glucemia basal, HbA1c y perfil lipídico. Indicación de realizar pruebas funcionales, básicamente test de tolerancia oral a la glucosa (TTOG):
- a) antecedentes familiares en primer grado de diabetes tipo 2;
- b) glucemia basal alterada (100-125 mg/dl) o HbA1c >6-6,5%;
- c) obesidad, y
- d) otros datos que completen o creen riesgo de síndrome metabólico: hipertensión, dislipemia (triglicéridos >150mg/dl o colesterol HDL <35 en hombres/<39 en mujeres), microalbuminuria.
Respecto a la donación:
- El antecedente o diagnóstico de diabetes (glucemia basal >126 en dos ocasiones o glucemia casual o a las 2 horas del TTOG >200) es una contraindicación absoluta para la donación.
- El antecedente de diabetes gestacional es una contraindicación absoluta, dada la elevada tasa de desarrollo tardío de diabetes.
- La glucemia basal alterada y la intolerancia hidrocarbonada (glucemia a las 2 horas entre 140 y 199) son una contraindicación relativa y deben ser valoradas individualmente, teniendo en cuenta la respuesta a un plan de intervención sencillo (dieta, ejercicio, estatinas). La glucemia basal alterada en el rango alto (110-125), los antecedentes familiares, la presencia de otros factores de riesgo o de síndrome metabólico predicen mayor tendencia al desarrollo posterior de diabetes y afectación renal y nos inclinarían a descartar la donación.
Respiratorio: Las pruebas de función respiratorias estarían indicadas ante una clínica indicativa de enfermedad pulmonar crónica y en grandes fumadores.
Detección de cáncer: Se hacen estudios de:
Colon: indicada según recomendaciones para la población general: antecedentes familiares en primer grado, edad >50 años y otros. Mínimo: sangre oculta en heces. Recomendable colonoscopia.
Mama: mamografía/ecografía para mujeres >40 años, o antes si hay antecedentes familiares.
Útero: citología cervical y ecografía genital.
Próstata: tacto rectal y antígeno prostático específico para hombres >50 años, o antes si hay antecedentes familiares de cáncer de próstata precoz.
Estudios específicos en función de los hallazgos del estudio preliminar o de antecedentes personales o familiares; por ejemplo: examen por dermatología si hay antecedentes familiares de melanoma o un número muy elevado de nevus.
La donación está descartada si hay diagnóstico previo de cáncer hematológico, gastrointestinal, testicular, melanoma, pulmonar, mamario, renal o urinario, coriocarcinoma o gammapatía monoclonal.
En casos seleccionados en los que el cáncer se considere curado y sin riesgo de transmisión puede contemplarse la donación, tras discusión con la pareja.

La principal indicación del trasplante renal de vivo es el trasplante anticipado (preemptive). Éste permitirá al paciente librarse de las complicaciones de la diálisis y, además está demostrado que tiene mejores resultados que el trasplante realizado cuando ya se ha iniciado la diálisis.
Son también indicaciones prioritarias de trasplante renal de vivo los gemelos univitelinos y los hermanos HLA idénticos. Además, tendremos condiciones muy favorables cuando el donante es joven y hombre.

Estos enfermos se pueden beneficiar de una donación de vivo de los hermanos HLA idénticos o de los que comparten un haplotipo o de los padres. Si con todos los familiares la prueba cruzada sigue dando positiva entonces lo ideal es entrar en programas de trasplante renal de hiperinmunizados compartiendo donantes fallecidos o en programas de trasplante renal de vivo cruzado. Antes puede ensayarse en estos pacientes terapias de desensibilización para comprobar si se negativiza la prueba cruzada con los donantes vivos.
La mejor terapéutica para los pacientes con diabetes mellitus tipo 1 e insuficiencia renal terminal es un trasplante simultáneo de páncreas y riñón, idealmente anticipado, con órganos del mismo donante fallecido. Desgraciadamente la escasez de donantes de páncreas es muy acusada, dado que los criterios de selección incluyen edades de donante muy jóvenes y sin apenas comorbilidad aguda. Esto hace que los pacientes pasen largos tiempos en diálisis esperando el trasplante simultáneo.
Una alternativa al trasplante simultáneo de páncreas y riñón para diabéticos tipo 1 con fallo renal es el trasplante secuencial de riñón de un donante vivo seguido de un trasplante de páncreas de un donante fallecido. Esta estrategia terapéutica tendría la ventaja de poder hacer el trasplante de vivo de forma anticipada evitando la morbilidad de la diálisis
Los pacientes con enfermedades renales con alta tasa de recidiva tras el trasplante tienen una contraindicación absoluta para la donación renal de vivo. Pueden ser relativas en un primer trasplante pero si en éste se produce la recidiva de la enfermedad renal primaria y esto es la causa de la pérdida del injerto, la contraindicación es absoluta para un segundo trasplante.
En el trasplante renal la edad del donante y el tamaño del injerto son factores conocidos que condicionan la evolución del injerto a largo plazo. Las mujeres tienden a tener unos riñones más pequeños, con un 17% menos de nefronas que los hombres. El número de nefronas por riñón tiene una correlación positiva con el peso del riñón y negativa con la edad del individuo. Se ha descrito que el sexo femenino del donante por el menor tamaño de los riñones influye negativamente en la evolución de los injertos cuando éstos son trasplantados a hombres.
En conjunto, las evidencias actuales nos dicen que cuando el donante es femenino y la edad es avanzada y el receptor es hombre y joven no estamos ante las circunstancias más adecuadas para garantizar unos buenos resultados a medio y largo plazo. Por tanto, este emparejamiento donante-receptor supondría una contraindicación relativa para la donación renal de vivo. Y como tal contraindicación relativa, si finalmente se considera oportuno realizar el trasplante de vivo con este tipo de donante, deberá ser tras una información exhaustiva sobre los riesgos a donante y a receptor.
En general, estas condiciones más desfavorables podrían tener menos importancia si lo que se está planteando es la realización de un trasplante anticipado, ya que las ventajas de no pasar por diálisis probablemente compensen, al menos en parte, los inconvenientes de estos tipos de parejas donante-receptor.
Las causas de mortalidad a largo plazo en los donantes renales son similares a las observadas en la población general, siendo las complicaciones cardiovasculares, las neoplasias y los accidentes de tráfico las más frecuentes.
La incidencia de mortalidad es, de hecho, inferior a la esperada en relación con la de población general, ajustada por edad y sexo.
La nefrectomía unilateral realizada a una persona sana, por lo tanto con función renal excelente y sin factores de riesgo añadidos (HTA, obesidad, diabetes, etc.), no comporta un riesgo de nefropatía a largo plazo. Las sucesivas revisiones de series muy amplias y con un intervalo de seguimiento largo así lo demuestran.
La edad avanzada en el momento de la donación puede influir en el deterioro de la función renal a largo plazo, pero de forma similar a lo que se observa en la población general conforme avanza la edad.
Hipertensión arterial
La incidencia de HTA en las series de donantes controlados a largo plazo es similar a la observada en la población general y se detecta con mayor frecuencia, como era de esperar, en los donantes de mayor edad.
Es recomendable que los donantes realicen controles periódicos de tensión arterial, pues la detección precoz de la misma permite un tratamiento adecuado y previene el desarrollo de complicaciones más graves.
Hipertensión gestacional posdonación
Recientemente han aparecido dos publicaciones que estudian la posible relación de la donación renal en la aparición de problemas gestacionales. Reisaeter et al. revisan la experiencia con donantes noruegas y llegan a la conclusión que la incidencia de preeclampsia es más frecuente en las donantes después de la donación que antes de ella y también más frecuente
que en un grupo control de mujeres no donantes. Por su parte, Ibrahim et al. publican la experiencia de la Clínica Mayo y concluyen que también sus donantes presentan una mayor incidencia de preeclampsia, de hipertensión gestacional y de diabetes gestacional tras la donación que antes de ella. En ambos casos se trata de estudios retrospectivos que abren un interrogante y que invitan a analizar de forma más detenida esta cuestión, por si fuera necesario tenerla en cuenta a la hora de informar a las potenciales donantes.
Proteinuria
La reducción de la masa renal como consecuencia de la nefrectomía aumenta mínimamente la excreción de proteínas en orina. Pero la incidencia de proteinuria a largo plazo en donantes renales resulta muy variable según las series publicadas.
De nuevo hay que insistir en la importancia que podría tener la detección precoz de proteinuria, pues el tratamiento con inhibidores de la síntesis de angiotensina (IECA) o antagonistas del receptor de angiotensina (ARA), administrado precozmente, puede ser especialmente útil.
Insuficiencia renal
La función renal del riñón remanente suple de forma satisfactoria la disminución de masa renal. Normalmente la creatinina sérica y el filtrado glomerular alcanzan un 70-80% del valor previo a la nefrectomía y se mantienen estables a lo largo de los años. En donantes de edad avanzada o con filtrado en el límite bajo de la normalidad es posible observar valores de
creatinina sérica discretamente afectados. Acorto plazo, la recuperación de la función renal es peor conforme aumenta la edad en el momento de la donación, el índice de masa corporal y especialmente cuanto más bajo es el filtrado glomerular antes de la donación. Los donantes de raza negra también presentan una menor recuperación del filtrado glomerular basal.
Actualmente se recomienda llevar a cabo un seguimiento prospectivo y sistemático a largo plazo de los donantes y tratar precozmente a los individuos que desarrollen hipertensión arterial.
Otras cuestiones a tener en cuenta
Actualmente uno de los principales y más preocupantes motivos de pérdida de injertos renales, es el rechazo provocado por el abandono o toma irregular de la medicación inmunosupresora. Este medicación debe tomarse de forma estricta para evitar estos sucesos, que pueden terminar con la pérdida del injerto.
Los pacientes que reciben un riñón de un dónate en asitolia, suelen requerir mayor tiempo de estancia hospitalaria, dadas las características de este tipo de trasplante.
Es importante señalar que durante los primeros días posteriores al trasplante el paciente requiere ser ingresado en la UCI y/o unidades de aislamiento(viendo reducido el contacto con sus familiares) debido a la inmunosupresión al que es somentido.
